Bài 33: Điều chế khí hiđro - phản ứng thế
I. ĐIỀU CHẾ KHÍ HIĐRO
1. Trong phòng thí nghiệm
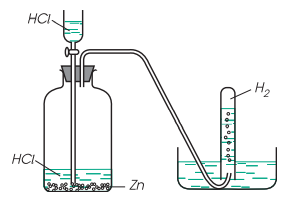
- Khí $H_{2}$ được điều chế bằng cách: cho axit ($HCl$ hoặc $H_{2}SO_{4}$ loãng…) tác dụng với kim loại $(Zn, \,Al, \,Fe,…).$
- Phương trình hóa học:
$Zn\,\, + \,\,2\,HCl\,\, \longrightarrow \,\,ZnCl_{2}\,\, + \,\,H_{2}\,\uparrow$
- Nhận biết khí $H_{2}$ bằng que đóm đang cháy (cháy trong không khí với ngọn lửa xanh nhạt), hoặc dùng tàn đóm (không làm tàn đóm bùng cháy).
- Thu khí $H_{2}$ bằng cách:
+ Đẩy nước.
+ Đẩy không khí.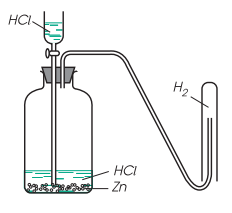
2. Trong công nghiệp
- Hiđro được điều chế bằng cách điện phân nước hoặc dùng than khử oxi của $H_{2}O$ trong lò khí than hoặc điều chế $H_{2}$ từ khí tự nhiên, khí dầu mỏ.
$2\,H_{2}O\,\,\,\, {\overset{điện\,\,phân}{\longrightarrow}} \,\,\,\,2\,H_{2}\,\uparrow \,\, + \,\,O_{2}\,\uparrow$
II. PHẢN ỨNG THẾ
- Phản ứng thế là phản ứng hóa học giữa đơn chất và hợp chất, trong đó nguyên tử của đơn chất thay thế nguyên tử của một nguyên tố khác trong hợp chất.
Ví dụ:
$Zn\,\, + \,\,2\,HCl\,\, \longrightarrow \,\,ZnCl_{2}\,\, + \,\,H_{2}\,\uparrow$
$Fe\,\, + \,\,H_{2}SO_{4}\,\, \longrightarrow \,\,FeSO_{4}\,\, + \,\,H_{2}\,\uparrow$