Bài 32. Ankin
I - ĐỒNG ĐẲNG, ĐỒNG PHÂN, DANH PHÁP
1. Dãy đồng đẳng ankin
Axetilen $(CH \equiv CH)$ và các chất tiếp theo có công thức phân tử ${C_3}{H_4},{\rm{ }}{C_4}{H_6},{\rm{ }}...$ có tính chất tương tự axetilen lập thành dãy đồng đẳng của axetilen được gọi là ankin. Công thức phân tử chung của ankin là ${C_n}{H_{2n - 2}}{\rm{ }}\left( {n \ge 2} \right)$.
Cấu tạo của phân tử axetilen:
${\rm{H:C}} \vdots \vdots {\rm{C:H}}$
Công thức electron
${\rm{H - C}} \equiv {\rm{C - H}}$
Công thức cấu tạo
2. Đồng phân
Hai chất đầu dãy $\left( {{C_2}{H_2},{\rm{ }}{C_3}{H_4}} \right)$ không có đồng phân ankin. Các ankin từ ${C_4}{H_6}$ trở lên có đồng phân vị trí của liên kết ba, từ ${C_5}{H_8}$ còn có đồng phân mạch cacbon (tương tự anken).
3. Danh pháp
a) Tên thông thường
Tên gốc ankyl liên kết với nguyên tử C của liên kết ba + axetilen
b) Tên thay thế
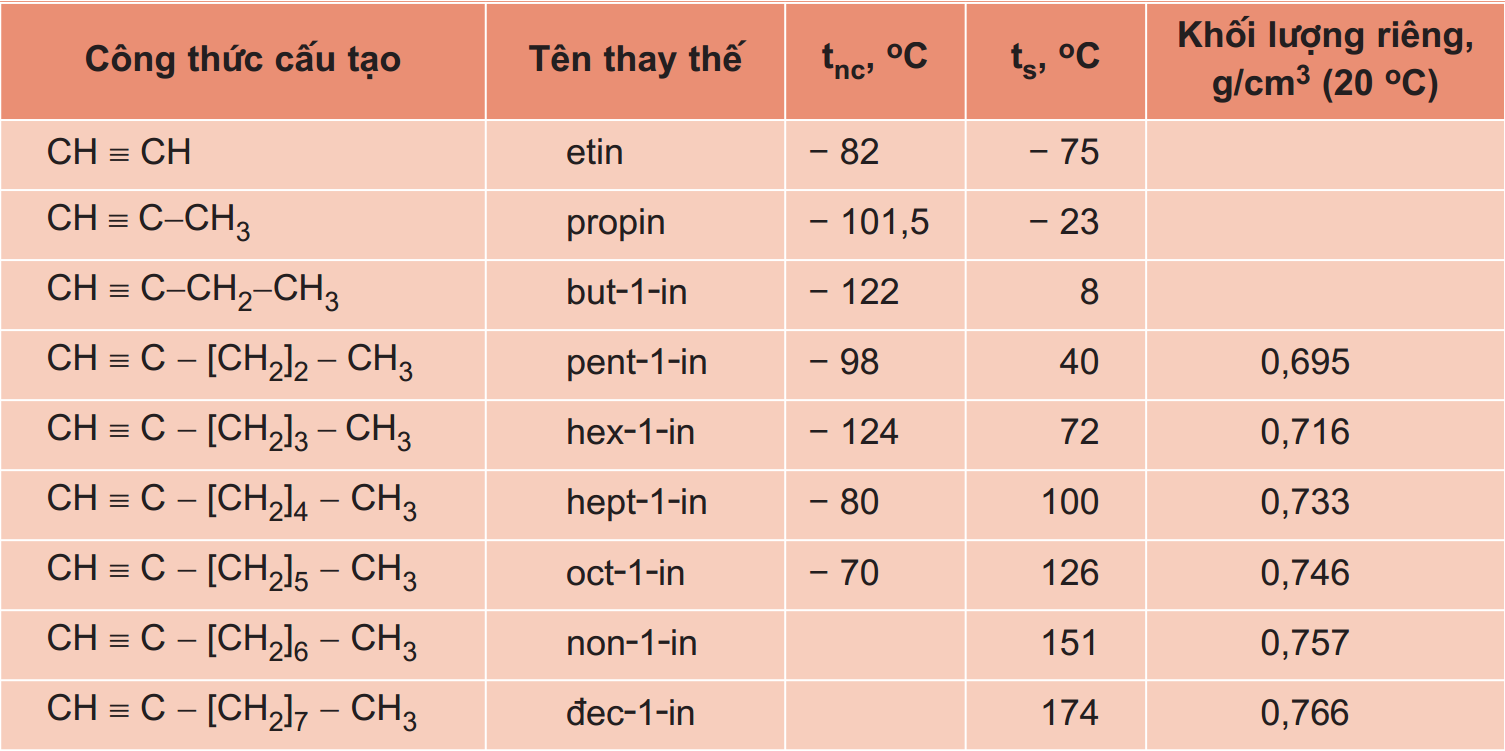
Các ankin có liên kết ba ở đầu mạch (dạng ${\rm{R}} - C \equiv CH$) được gọi là các ank-1-in.
II. TÍNH CHẤT VẬT LÍ
Ankin có nhiệt độ sôi tăng dần theo chiều tăng của phân tử khối. Các ankin có nhiệt độ sôi cao hơn và khối lượng riêng lớn hơn các anken tương ứng.
Giống ankan và anken, các ankin cũng không tan trong nước và nhẹ hơn nước.
III. TÍNH CHẤT HOÁ HỌC
1. Phản ứng công
a) Cộng hiđro
Khi có niken (hoặc platin hoặc palađi) làm xúc tác, ankin cộng hiđro tạo thành anken, sau đó tạo thành ankan.
Khi dùng xúc tác là hỗn hợp $Pd/PbC{O_3}$ hoặc $Pd/BaS{O_4}$, ankin chỉ cộng một phân tử hiđro tạo thành anken.
Đặc tính này được dùng để điều chế anken từ ankin.
b) Cộng brom, clo
Brom và clo cũng tác dụng với ankin theo hai giai đoạn liên tiếp.
c) Cộng HX ($X$là ${\rm{ }}OH,{\rm{ }}Cl,{\rm{ }}Br,{\rm{ }}C{H_3}COO...$)
Ankin tác dụng với HX theo hai giai đoạn liên tiếp.
Khi có xúc tác thích hợp, ankin tác dụng với HCl sinh ra dẫn xuất monoclo của anken.
Phản ứng cộng HX của các ankin cũng tuân theo quy tắc Mac-côp-nhi-côp.
Phản ứng cộng ${H_2}O$ của các ankin chỉ xảy ra theo tỉ lệ số mol 1 : 1.
d) Phản ứng đime và trime hoá
Hai phân tử axetilen cộng hợp với nhau tạo thành vinylaxetilen :
$CH \equiv CH + 2AgN{O_3} + 2N{H_3} \to $
$ \to Ag - C \equiv C - Ag \downarrow + 2N{H_4}N{O_3}$
bạc axetilua
$\to Ag - C \equiv C - Ag \downarrow + 2N{H_4}N{O_3}$
bạc axetilua
b) Nhận xét:
Nguyên tử hiđro liên kết trực tiếp với nguyên tử cacbon liên kết ba đầu mạch có tính linh động cao hơn các nguyên tử hiđro khác nên có thể bị thay thế bằng ion kim loại.
Các ank-1-in khác như propin, but-1-in, ... cũng có phản ứng tương tự axetilen, do đó tính chất này được dùng để phân biệt ank-1-in với anken và các ankin khác.
3. Phản ứng oxi hoá
a) Phản ứng oxi hoá hoàn toàn (cháy)
Các ankin cháy toả nhiều nhiệt:
$2{C_n}{H_{2n - 2}} + {\rm{ }}\left( {3n{\rm{ }} - {\rm{ }}1} \right){O^2}2nC{O_2} + {\rm{ }}2\left( {n{\rm{ }} - {\rm{ }}1} \right){H_2}O$
b) Phản ứng oxi hoá không hoàn toàn
Tương tự anken và ankađien, ankin cũng có khả năng làm mất màu dung dịch thuốc tím.
IV. ĐIỀU CHẾ
Trong phòng thí nghiệm và trước đây cả trong công nghiệp, axetilen được điều chế bằng cách cho canxi cacbua $Ca{C_2}$ tác dụng với nước :
$Ca{C_2} + {\rm{ }}2{H_2}O{C_2}{H_2} \uparrow + {\rm{ }}Ca{(OH)_2}$
Ngày nay trong công nghiệp, axetilen được sản xuất chủ yếu từ metan:
${\rm{2C}}{{\rm{H}}_{\rm{4}}}{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{2}}}{\rm{ + 3}}{{\rm{H}}_{\rm{2}}}$
V. ỨNG DỤNG
1. Làm nhiên liệu
Khi cháy, axetilen toả nhiều nhiệt nên được dùng trong đèn xì oxi-axetilen để hàn, cắt kim loại.
2. Làm nguyên liệu
Từ axetilen có thể điều chế được nhiều chất đầu quan trọng cho các quá trình tổng hợp hữu cơ.
1. Dãy đồng đẳng ankin
Axetilen $(CH \equiv CH)$ và các chất tiếp theo có công thức phân tử ${C_3}{H_4},{\rm{ }}{C_4}{H_6},{\rm{ }}...$ có tính chất tương tự axetilen lập thành dãy đồng đẳng của axetilen được gọi là ankin. Công thức phân tử chung của ankin là ${C_n}{H_{2n - 2}}{\rm{ }}\left( {n \ge 2} \right)$.
Cấu tạo của phân tử axetilen:
${\rm{H:C}} \vdots \vdots {\rm{C:H}}$
Công thức electron
${\rm{H - C}} \equiv {\rm{C - H}}$
Công thức cấu tạo
2. Đồng phân
Hai chất đầu dãy $\left( {{C_2}{H_2},{\rm{ }}{C_3}{H_4}} \right)$ không có đồng phân ankin. Các ankin từ ${C_4}{H_6}$ trở lên có đồng phân vị trí của liên kết ba, từ ${C_5}{H_8}$ còn có đồng phân mạch cacbon (tương tự anken).
3. Danh pháp
a) Tên thông thường
Tên gốc ankyl liên kết với nguyên tử C của liên kết ba + axetilen
b) Tên thay thế

Các ankin có liên kết ba ở đầu mạch (dạng ${\rm{R}} - C \equiv CH$) được gọi là các ank-1-in.
II. TÍNH CHẤT VẬT LÍ
Ankin có nhiệt độ sôi tăng dần theo chiều tăng của phân tử khối. Các ankin có nhiệt độ sôi cao hơn và khối lượng riêng lớn hơn các anken tương ứng.
Giống ankan và anken, các ankin cũng không tan trong nước và nhẹ hơn nước.
III. TÍNH CHẤT HOÁ HỌC
1. Phản ứng công
a) Cộng hiđro
Khi có niken (hoặc platin hoặc palađi) làm xúc tác, ankin cộng hiđro tạo thành anken, sau đó tạo thành ankan.
Khi dùng xúc tác là hỗn hợp $Pd/PbC{O_3}$ hoặc $Pd/BaS{O_4}$, ankin chỉ cộng một phân tử hiđro tạo thành anken.
Đặc tính này được dùng để điều chế anken từ ankin.
b) Cộng brom, clo
Brom và clo cũng tác dụng với ankin theo hai giai đoạn liên tiếp.
c) Cộng HX ($X$là ${\rm{ }}OH,{\rm{ }}Cl,{\rm{ }}Br,{\rm{ }}C{H_3}COO...$)
Ankin tác dụng với HX theo hai giai đoạn liên tiếp.
Khi có xúc tác thích hợp, ankin tác dụng với HCl sinh ra dẫn xuất monoclo của anken.
Phản ứng cộng HX của các ankin cũng tuân theo quy tắc Mac-côp-nhi-côp.
Phản ứng cộng ${H_2}O$ của các ankin chỉ xảy ra theo tỉ lệ số mol 1 : 1.
d) Phản ứng đime và trime hoá
Hai phân tử axetilen cộng hợp với nhau tạo thành vinylaxetilen :
$CH \equiv CH + 2AgN{O_3} + 2N{H_3} \to $
$ \to Ag - C \equiv C - Ag \downarrow + 2N{H_4}N{O_3}$
bạc axetilua
Ba phân tử axetilen cộng hợp với nhau tạo thành benzen:
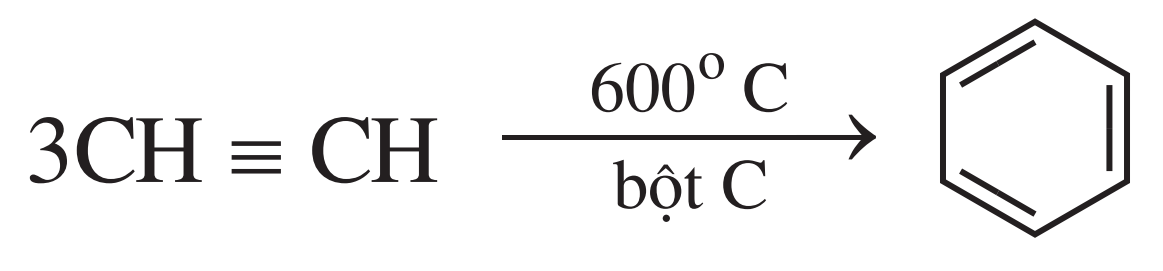
Về hình thức, đây cũng là phản ứng cộng HX vào liên kết ba, với HX là $H - C \equiv CH.
2. Phản ứng thế bằng ion kim loại
a) Thí nghiệm:
Sục khí
axetilen vào dung dịch bạc nitrat trong amoniac, thấy có kết tủa vàng nhạt. Đó là muối bạc axetilua tạo thành do phản ứng:
$\to Ag - C \equiv C - Ag \downarrow + 2N{H_4}N{O_3}$
bạc axetilua
b) Nhận xét:
Nguyên tử hiđro liên kết trực tiếp với nguyên tử cacbon liên kết ba đầu mạch có tính linh động cao hơn các nguyên tử hiđro khác nên có thể bị thay thế bằng ion kim loại.
Các ank-1-in khác như propin, but-1-in, ... cũng có phản ứng tương tự axetilen, do đó tính chất này được dùng để phân biệt ank-1-in với anken và các ankin khác.
3. Phản ứng oxi hoá
a) Phản ứng oxi hoá hoàn toàn (cháy)
Các ankin cháy toả nhiều nhiệt:
$2{C_n}{H_{2n - 2}} + {\rm{ }}\left( {3n{\rm{ }} - {\rm{ }}1} \right){O^2}2nC{O_2} + {\rm{ }}2\left( {n{\rm{ }} - {\rm{ }}1} \right){H_2}O$
b) Phản ứng oxi hoá không hoàn toàn
Tương tự anken và ankađien, ankin cũng có khả năng làm mất màu dung dịch thuốc tím.
IV. ĐIỀU CHẾ
Trong phòng thí nghiệm và trước đây cả trong công nghiệp, axetilen được điều chế bằng cách cho canxi cacbua $Ca{C_2}$ tác dụng với nước :
$Ca{C_2} + {\rm{ }}2{H_2}O{C_2}{H_2} \uparrow + {\rm{ }}Ca{(OH)_2}$
Ngày nay trong công nghiệp, axetilen được sản xuất chủ yếu từ metan:
${\rm{2C}}{{\rm{H}}_{\rm{4}}}{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{2}}}{\rm{ + 3}}{{\rm{H}}_{\rm{2}}}$
V. ỨNG DỤNG
1. Làm nhiên liệu
Khi cháy, axetilen toả nhiều nhiệt nên được dùng trong đèn xì oxi-axetilen để hàn, cắt kim loại.
2. Làm nguyên liệu
Từ axetilen có thể điều chế được nhiều chất đầu quan trọng cho các quá trình tổng hợp hữu cơ.



