Bài 30. Silic. Công nghiệp silicat
I. SILIC
Kí hiệu hóa học: $Si$
Nguyên tử khối: $28$
1. Trạng thái thiên nhiên
- Silic là nguyên tố phổ biến thứ hai trong thiên nhiên, chỉ sau oxi. Silic chiếm ¼ khối lượng vỏ Trái Đất.
- Trong tự nhiên, silic không tồn tại ở dạng đơn chất mà chỉ tồn tại ở dạng hợp chất. Các hợp chất của silic tồn tại nhiều là cát trắng, đất sét (cao lanh).
2. Tính chất
- Silic là chất rắn, màu xám, khó nóng chảy, có vẻ sáng của kim loại, dẫn điện kém. Tinh thể silic tinh khiết là chất bán dẫn.
- Silic là phi kim hoạt động hóa học yếu hơn cacbon, clo. Ở nhiệt độ cao, silic phản ứng với oxi tạo thành silic đioxit
$Si\,\,{}_{(r)}\,\, + \,\,O_{2}\,\,{}_{(k)}\,\, {\overset{t^o}{\longrightarrow}} \,\,SiO_{2}\,\,{}_{(r)}$
- Silic được dùng làm vật liệu bán dẫn trong kĩ thuật điện tử và được dùng để chế tạo pin mặt trời...
II. SILIC ĐIOXIT $(SiO_{2})$
- $SiO_{2}$ là oxit axit, tác dụng với kiềm và oxit bazơ tan tạo thành muối silicat ở nhiệt độ cao.
$SiO_{2}\,\,{}_{(r)}\,\, + \,\,2\,NaOH\,\,{}_{(r)}\,\, {\overset{t^o}{\longrightarrow}} \,\,\underbrace {\mathop {Na_{2}SiO_{3}}\limits_{}^{}\,\,{}_{(r)}}_{\mathop {(Natri\,\,silicat)}\limits_{}^{}}\,\, + \,\,H_{2}O\,\,{}_{(h)}$
$SiO_{2}\,\,{}_{(r)}\,\, + \,\,CaO\,\,{}_{(r)}\,\, {\overset{t^o}{\longrightarrow}} \,\,\underbrace {\mathop {CaSiO_{3}}\limits_{}^{}\,\,{}_{(r)}}_{\mathop {(Canxi\,\,silicat)}\limits_{}^{}}$
- Silic đioxit không phản ứng với nước.
III. SƠ LƯỢC VỀ CÔNG NGHIỆP SILICAT
1. Sản xuất đồ gốm
- Đồ gốm gồm: gạch ngói, gạch chịu lửa, sành, sứ.
a) Nguyên liệu chính:
- Đất sét, thạch anh, fenpat.
b) Các công đoạn chính:
- Nhào đất sét, thạch anh và fenpat với nước, tạo thành khối dẻo rồi tạo hình thành đồ vật và sấy khô.
- Nung các đồ vật trong lò ở nhiệt độ cao thích hợp.
c) Cơ sở sản xuất:
- Ở nước ta có nhiều cơ sở sản xuất gốm, sứ như: Bát Tràng (Hà Nội), Hải Dương, Đồng Nai, Sông Bé,…
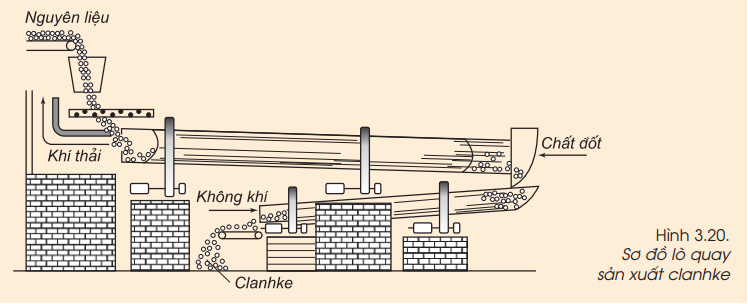
2. Sản xuất xi măng
- Xi măng là nguyên liệu kết dính trong xây dựng. Thành phần chính của xi măng là canxi silicat và canxi aluminat.
a) Nguyên liệu chính:
- Đất sét, đá vôi, cát,...
b) Các công đoạn chính:
- Nghiền nhỏ hỗn hợp đá vôi và đất sét rồi trộn với cát và nước ở dạng bùn.
- Nung hỗn hợp trên lò quay (lò đứng) ở $1.400-1.500^{o}C,$ thu được clanhke rắn.
- Nghiền clanhke nguội với phụ gia thành bột mịn, đó là xi măng.
c) Cơ sở sản xuất:
- Nước ta có các nhà máy xi măng ở Hải Dương, Thanh Hóa, Hải Phòng, Hà Nam, Nghệ An, Hà Tiên,…
3. Sản xuất thủy tinh
- Thành phần chính của thủy tinh thường gồm hỗn hợp của silicat $(Na_{2}SiO_{3})$ và canxi silicat $(CaSiO_{3}).$
a) Nguyên liệu chính:
- Cát thạch anh (cát trắng), đá vôi và sôđa $(Na_{2}CO_{3}).$
b) Các công đoạn chính:
- Trộn hỗn hợp nguyên liệu cát, đá vôi, sôđa theo tỉ lệ thích hợp.
- Nung hỗn hợp trong lò nung ở khoảng $900^{o}C,$ thu được thủy tinh nhão.
- Làm nguội từ từ được thủy tinh dẻo.
- Ép, thổi thủy tinh dẻo thành các đồ vật.
- Các phương trình hóa học:
$CaCO_{3}\,\,{}_{(r)}\,\, {\overset{t^o}{\longrightarrow}} \,\,CaO\,\,{}_{(r)}\,\, + \,\,CO_{2}\,\,{}_{(k)}$
$CaO\,\,{}_{(r)}\,\, + \,\,SiO_{2}\,\,{}_{(r)}\,\, {\overset{t^o}{\longrightarrow}} \,\,CaSiO_{3}\,\,{}_{(r)}$
$Na_{2}CO_{3}\,\,{}_{(r)}\,\, + \,\,SiO_{2}\,\,{}_{(r)}\,\, {\overset{t^o}{\longrightarrow}} \,\,Na_{2}SiO_{3}\,\,{}_{(r)}\,\, + \,\,CO_{2}\,\,{}_{(k)}$
c) Cơ sở sản xuất:
- Nước ta có các nhà máy sản xuất thủy tinh ở Hải Phòng, Hà Nội, Bắc Ninh, Đà Nẵng, Thành phố Hồ Chí Minh,...